国际帕金森病与运动障碍协会 (IPMDS) 工作组将帕金森病定义为“伴有黑质致密部神经元变性和α-突触核蛋白沉积的核心临床运动综合征(帕金森综合征)。
不过,这种临床病理实体无法在死前得到验证,因此,在没有其他诊断指标(如非典型帕金森综合征)的情况下,诊断依据是典型的帕金森运动特征。
但随着相关研究进一步完善,也挖掘出了一些新的诊断方法。
最新的研究发现,α-突触核蛋白种子扩增试验可准确区分帕金森病和健康对照组,并且可以识别疾病的不同阶段[3]。

目前也在进一步开发新的帕金森病生物标志物定义,以便在生物学基础上诊断帕金森病。
但这种生物标志物在鉴别帕金森病与其他非典型帕金森综合征中的实际应用价值,还需进一步验证。
另外,IPMDS也指出,一些特定的会造成帕金森病的基因突变,也可以作为帕金森病的辅助诊断。
目前确定了七种单基因突变与帕金森病显著相关,其中包括四种晚发、常染色体显性遗传型(如LRRK2、CHCHD2、VPS35、SNCA),以及三种早发、常染色体隐性遗传型(PARKIN、DJ1、PINK1)。虽然基因检测目前并非帕金森病诊断的核心手段,但它有助于明确患者的预后并指导家族成员的风险评估。
2.1 时间的影响
随着人们寿命的延长,帕金森病患者的数量也在增加,并且预计将继续增加。一项对2016年全球疾病负担研究数据的系统分析估计,帕金森粗略患病率在1990年至2016年间增加了约74%。
尽管大多数地区患病率均有所上升,但观察到的患病率和死亡率在时间和空间上都存在显著差异。预计大部分增长将在低收入和中等收入国家发生。
帕金森病在全球不同地区间的患病率存在显著异质性。例如,在欧洲和北美地区的患病率较高,而非洲、亚洲部分地区则较低。
这些差异可能与遗传变异、 地理因素、环境因素、基因与环境交互作用、获得卫生保健的机会、预期寿命以及研究方法的不同有关。
但可能也与非洲、亚洲等地医疗资源和社会经济状况较欧美国家差,导致患病者未能被及时诊断有关。
随着年龄的增长,帕金森病的风险也会增加。在EUROPARKINSON研究中,未诊断出的病例比例从65-70岁年龄组的18%增加到80-85岁年龄组的36%。
目前尚不清楚与年龄有关的细胞死亡是否是生物老化不可避免的功能,还是慢性接触环境毒素的结果。在大多数情况下,衰老相关的细胞变化、遗传决定的过程和环境损伤之间的复杂相互作用可能是导致神经退行性病变的原因。
男性帕金森病的发病率、患病率和死亡风险高于女性,比例约为1.4:1。相关的流行病学调查也佐证了这一观点。
如罗切斯特流行病学项目发现,男性的发病率在1976-1985年以及1996-2005年期间有所增加,但女性的发病率保持稳定。
男性发病率较高的原因尚不完全清楚,可能的假设包括男性暴露于不良环境风险因素较多,以及雌激素的保护作用等。
社会经济地位与疾病风险之间存在显著差异,总体而言,社会经济地位较低的人群患病风险更高,反映了他们在人的一生中遭受各种不良经历的风险更大。
但在不同的研究发现了不一致的结果,有研究表明在高收入国家,较高的社会经济地位的人无论目前或既往吸烟的几率更低。最近的孟德尔随机化分析发现,预测有更高的认知能力的遗传变异(单核苷酸多态性)增加了PD发病的风险,这点与阿尔茨海默氏症的观察结果正好相反。
疾病的决定因素可以是内在的或外在的。
帕金森病的大多数病例都是由环境暴露因素与调节代谢途径的基因变异共同作用引起的。
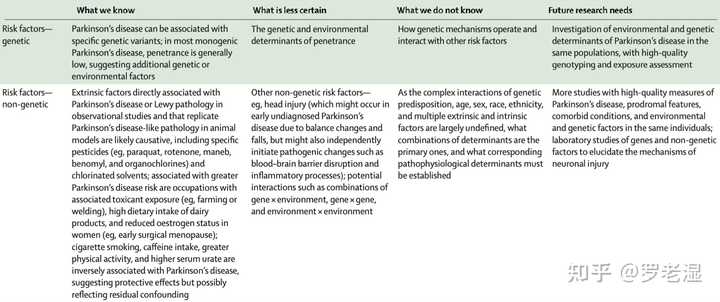
单卵双生子和双卵双生子一致性分析研究表明,帕金森病的遗传率仅为30%,这表明环境和行为因素在其中发挥更大作用。
环境因素在帕金森病发病中扮演着重要角色。据相关研究显示,长期接触神经毒性物质,如氯化溶剂(三氯乙烯、全氯乙烯和四氯化碳等),以及空气污染与人类帕金森病风险增加有关,并在动物模型中引起帕金森病相关毒性。
环境毒物暴露,如百草枯、鱼藤酮等杀虫剂,具有生化效应,可导致线粒体功能障碍、炎症、微生物组的改变,从而诱发帕金森病。
从狭义上讲,帕金森病是一种遗传性疾病,某些患者具有明确的罕见基因变异,可导致家族性疾病;从广义上讲,许多患者因一系列常见风险变异而具有多基因疾病风险。

3.2.1 家族性帕金森病
如SNCA、LRRK2、VPS35等基因的突变可导致常染色体显性和隐性遗传的帕金森病。
特别是SNCA基因编码的α-突触核蛋白过表达,不仅会导致蛋白质异常聚集,还可在某些家族中表现为早发且快速进展的临床表现。
3.2.2 多基因疾病
全基因组关联研究显示迄今为止,共有74个基因组位点的90个独立变异与疾病风险相关,每个变异都使帕金森病的风险略有增加。
如LRRK2 Gly2385Arg变异是中国和韩国人群帕金森病的危险因素,欧洲人群中的SNCA和MAPT基因位点,以及非洲人群中GBA1基因变异是公认的主要风险因素。
一项病例对照研究的荟萃分析表明,头部受伤与帕金森病有关。
友情提示:文中还一些观点可能会颠覆你的认知。
比如,吸烟对人体有害,但它却在帕金森病中表现出一定的“保护效应”,烟草的使用时间越长,频率越高,PD的风险越低。但具体机制尚不明确,还需进一步研究。
日常乳制品摄入量也与帕金森病的风险增加有关,这可能是由于牛奶中有毒物质富集所致。
具体可以看下——风险和保护因素如何决定神经病理学和帕金森病发展的简化示意图。

典型的帕金森病症状分为两大类,一类是运动症状,另一类是非运动症状。
通过科学的治疗策略,可以有效地缓解帕金森病的症状,提高患者的生活质量。
药物治疗是帕金森病的主要治疗方法之一。药物可以通过调节神经递质的含量和功能,缓解症状,提高患者的生活质量。常见的药物包括左旋多巴、多巴胺受体激动剂、MAO-B抑制剂等。
对于一些严重的帕金森病患者,药物治疗可能无法完全控制症状。此时,手术治疗可能是一个可行的选择。手术治疗包括脑深部电刺激、脑立体定向毁损术等,可以通过调节神经系统的功能,进一步缓解症状。
康复治疗是帕金森病治疗中不可或缺的一部分。康复治疗包括物理疗法、心理疗法、言语疗法等,可以帮助患者改善运动功能、提高生活自理能力、减轻心理压力等。
预防策略可分为一级、二级和三级。
一级预防着重于减少或消除可能导致帕金森病的风险因素。一级干预面向整个人群,以人群为基础。
6.1.1 减少环境暴露
上文3.1中提到了环境暴露可能增加帕金森病的风险,因此,减少接触这些有害物质,或者在接触之前做好自我保护措施是潜在的预防措施之一。
6.1.2 调节生活方式
6.1.3 公共卫生策略
应该建立针对帕金森病的综合性预防策略,包括普及公众教育、改善生活环境、促进健康老龄化政策以及强化职业防护措施,尤其在农业、化工等行业加强神经毒性物质的管理。
通过遗传风险标记物或帕金森病前驱症状,如嗅觉受损、快速眼动(REM)睡眠行为障碍和便秘,筛查出帕金森病高风险人群,在前驱期阶段干预,可能会延缓细胞变性或减缓其进展速度。
但是任何药物干预都需要平衡干预的成本和风险,因为高风险人群人也可能永远不会发展为临床帕金森病。
三级预防旨在延缓已确诊帕金森病患者的病情进展,提高生活质量,减轻并发症及死亡率。
这一层面的预防主要通过综合性的治疗方案来实现,包括药物治疗、神经调控疗法(如脑起搏器植入术)、物理疗法以及心理支持等。

在所有的预防措施中,二级预防最为重要,因为目前治疗帕金森病的药物研发和阿尔茨海默病一样困难。在所有的干预措施中,体育锻炼是性价比最高的。更重要的是,体育锻炼具有普适性,若扩大到全人口层面,体育锻炼可以预防现有帕金森病病例的14.5%。
未来,还需要进一步深入探讨帕金森病的病因和发病机制,为开发更加有效的预防和治疗策略提供理论支持。

